Trądzik różowaty: aktualizacja terapii farmakologicznej
Trądzik różowaty jest powszechnym przewlekłym dermatozem, który przede wszystkim dotyczy centralnej części twarzy, w tym policzków, nosa, oczu, brody i czoła.1 Podstawowe objawy skórne obejmują wrażliwość skóry, trwały rumień, grudki, krosty i teleangiektazje. Chociaż nasilenie objawów może się czasowo zmniejszać, w dłuższej perspektywie dermatoza u większości pacjentów ma tendencję do powolnego postępu.2
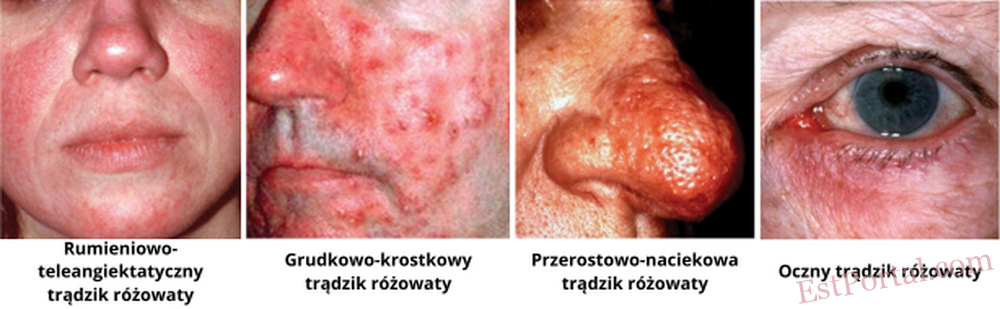
Narodowy Komitet ds. Trądziku Różowatego dzieli to schorzenie na cztery główne podtypy:
- rumieniowo-teleangiektatyczny,
- grudkowo-krostkowy,
- fimatoidalny,
- oczny.3
Możliwa jest transformacja jednego podtypu w inny.4 Prawidłowe określenie podtypów może pomóc w doborze strategii terapeutycznej.
Trądzik różowaty dotyka do 10% populacji ogólnej i zwykle pojawia się w wieku 30-50 lat.5 Jest szczególnie częsty wśród osób o jasnej karnacji pochodzenia północnoeuropejskiego.6 Częściej występuje u kobiet,5 jednak mężczyźni są bardziej podatni na rozwój zmian naciekowych i fimatoidalnych skóry, zwłaszcza w okolicy nosa.
Patofizjologia jest wieloczynnikowa i do końca niepoznana. Zaproponowano wiele czynników etiologicznych, w tym zaburzenia naczyniowe, problemy żołądkowo-jelitowe, degenerację macierzy skórnej, nieprawidłowości w funkcjonowaniu gruczołów łojowych, aktywność mikrobiologiczną oraz zmiany wrodzonej odpowiedzi immunologicznej.8,9
Trądzik różowaty może powodować problemy psychiczne, takie jak zawstydzenie, lęk i niska samoocena, co negatywnie wpływa na jakość życia. Te negatywne skutki powinny być uwzględnione w leczeniu pacjentów z trądzikiem różowatym.10,11
Konserwatywne metody leczenia, takie jak unikanie czynników wyzwalających, odpowiednia pielęgnacja skóry oraz stosowanie kosmetyków maskujących i ochrony przeciwsłonecznej, powinny być również elementami planu terapeutycznego.12
Standardowe metody leczenia
Miejscowy metronidazol
Metronidazol został po raz pierwszy zastosowany jako skuteczny lek na trądzik różowaty w 1980 roku.13 Chociaż metronidazol jest lekiem przeciwbakteryjnym i przeciwpasożytniczym, jego korzyści terapeutyczne w leczeniu trądziku różowatego wynikają głównie z jego właściwości przeciwzapalnych i przeciwutleniających.14 Wiele badań wykazało, że miejscowy metronidazol znacznie zmniejsza liczbę zmian zapalnych i zaczerwienie w porównaniu z placebo, jest dobrze tolerowany, ma niski poziom działań niepożądanych i skutecznie podtrzymuje remisję.15-18
Warto zauważyć, że różne formulacje metronidazolu, niezależnie od postaci (krem, żel lub lotion) czy stężenia (0,75% lub 1%)19-21, wykazują podobną skuteczność. Stosowanie metronidazolu raz dziennie okazało się tak samo skuteczne jak stosowanie dwa razy dziennie.19,22 Ponadto w połączeniu z filtrem przeciwsłonecznym SPF 15 metronidazol może zmniejszać rozwój teleangiektazji na twarzy.23 Należy zauważyć, że miejscowy metronidazol w przypadku stosowania u kobiet w ciąży klasyfikowany jest jako lek kategorii B.
Kwas azelainowy stosowany miejscowo
Kwas azelainowy jest naturalnym kwasem dikarboksylowym, zatwierdzonym w ostatniej dekadzie do leczenia łagodnej i umiarkowanej postaci trądziku różowatego.24 Najczęściej stosowany jest w postaci 15% żelu lub 20% kremu i wykazuje działanie terapeutyczne dzięki właściwościom przeciwzapalnym, antykeratolitycznym oraz antybakteryjnym.24 Kilka badań wykazało, że kwas azelainowy jest skuteczniejszy niż placebo w redukcji liczby zmian zapalnych i nasilenia rumienia.25-27
Zbiorcze wyniki pacjentów, którzy odnotowali znaczną poprawę po terapii kwasem azelainowym, wynosiły 70-80% w porównaniu do 50-55% w grupie placebo.28 Kwas azelainowy ma również stosunkowo niską częstotliwość działań niepożądanych, spośród których najczęściej zgłaszano pieczenie, mrowienie i podrażnienie.26 Częstość działań niepożądanych jest wyższa w przypadku kwasu azelainowego w porównaniu do metronidazolu, jednak efekty te są zazwyczaj łagodne i krótkotrwałe.29
Mimo że standardowy schemat stosowania kwasu azelainowego to aplikacja dwa razy dziennie, badania wykazały, że stosowanie raz dziennie jest równie skuteczne.30 Konieczne są dalsze badania w celu oceny stosowania kwasu azelainowego jako terapii podtrzymującej.28 W przypadku stosowania u kobiet w ciąży kwas azelainowy został zaklasyfikowany do kategorii B leków.
Tetracykliny
Stosowanie doustnych antybiotyków poza wskazaniami w leczeniu trądziku różowatego jest uznawane za skuteczne od ponad 50 lat. Korzyści terapeutyczne tetracyklin w trądziku różowatym wynikają głównie z ich działania przeciwzapalnego, a nie antybakteryjnego, ponieważ nie ma wystarczających dowodów na rolę infekcji bakteryjnej w patogenezie choroby.31 Antybiotyki z grupy tetracyklin są szczególnie zalecane w leczeniu trądziku różowatego ocznego, który występuje u ponad 50% pacjentów z tym schorzeniem.
Tetracykliny, które są przeciwwskazane u kobiet w ciąży, stanowią najczęściej stosowaną grupę antybiotyków i są szczególnie skuteczne w leczeniu zapalnych grudek i krost.
Tetracykliny drugiej generacji, w tym minocyklina i zwłaszcza doksycyklina, są szczególnie bezpieczne i skuteczne w leczeniu trądziku różowatego. W przeciwieństwie do tetracykliny charakteryzują się większą biodostępnością,32 szybszym początkiem działania i możliwością przyjmowania z posiłkiem, co minimalizuje skutki uboczne ze strony przewodu pokarmowego. Ponadto tetracykliny drugiej generacji wymagają jedynie jednokrotnego przyjmowania na dobę, co może poprawić przestrzeganie terapii przez pacjentów. Najważniejsze jest to, że są skuteczne w subantybiotykowych dawkach, co pozwala uniknąć negatywnego wpływu na florę bakteryjną i, co kluczowe, ogranicza ryzyko rozwoju oporności na antybiotyki.33
W niedawnych badaniach klinicznych33 wykazano, że subantybiotykowe dawki doksycykliny (40 mg na dobę) u pacjentów z umiarkowaną i ciężką postacią trądziku różowatego znacząco zmniejszały liczbę zapalnych grudek i krost w porównaniu z placebo po 16 tygodniach terapii, a istotna poprawa była widoczna już w 3. tygodniu. Częstość działań niepożądanych była niska i jedynie nieznacznie wyższa niż w grupie placebo. Do najczęstszych działań niepożądanych należały zapalenie nosogardzieli (4,8%), biegunka (4,4%) i bóle głowy (4,4%). Nie odnotowano przypadków nadwrażliwości na światło ani kandydozy pochwy.
W osobnym badaniu wykazano, że skuteczność terapii 40 mg doksycykliny jest porównywalna z terapią 100 mg doksycykliny.34 Subantybiotykowa dawka 40 mg doksycykliny została zatwierdzona w USA i Kanadzie do leczenia trądziku różowatego. W przeciwieństwie do tego, minocyklina nie została zatwierdzona, ponieważ w porównaniu z doksycykliną powoduje pięciokrotnie więcej działań niepożądanych, w tym hiperpigmentację, hepatotoksyczność i polekowy toczeń rumieniowaty.35
Dalsze badania są konieczne, aby ocenić skuteczność terapii skojarzonej subantybiotykowymi dawkami doksycykliny i miejscowego metronidazolu, przy której zaobserwowano szybszy początek działania i szybszą redukcję zmian zapalnych w porównaniu z monoterapią metronidazolem.36
Nowe i niedawno wprowadzone metody terapii
Miejscowy iwermektyna
Kilka miejscowych środków akarycydowych (permetryna 5%, krotamiton 10% i iwermektyna 1%) zostało przebadanych jako leki do leczenia trądziku różowatego. Wszystkie one wykazują zdolność do eliminowania roztoczy Demodex folliculorum i Demodex brevis. Potencjalna rola tych roztoczy w etiologii trądziku różowatego jest przedmiotem badań od wielu lat.9 Obserwuje się ponowny wzrost zainteresowania tymi roztoczami w związku z najnowszymi badaniami, które wykazały, że antygenowe białka wytwarzane przez bakterie symbiotyczne dla roztoczy (Bacillus oleronius) mogą nasilać reakcje zapalne w grudkowo-krostkowej, rumieniowo-teleangiektatycznej38 i ocznej postaci trądziku różowatego.37 Ten patogenny mechanizm, w którym kluczową rolę odgrywają bakterie Bacillus oleronius, a nie same roztocza, może tłumaczyć skuteczność antybiotyków w leczeniu trądziku różowatego.
Opublikowano liczne doniesienia39-41 o przypadkach skutecznego leczenia trądziku różowatego miejscowymi środkami akarycydowymi, jednak brakuje kontrolowanych badań randomizowanych. Obecnie trwa trzecia faza badań klinicznych oceniających skuteczność i bezpieczeństwo 1% kremu z iwermektyną w porównaniu z 0,75% kremem z metronidazolem i 15% żelem z kwasem azelainowym w leczeniu trądziku różowatego.42-44 Wyniki tych badań powinny być dostępne w najbliższym czasie.
Miejscowy brymonidyna i oksymetazolina
Rozlany i utrzymujący się rumień twarzy od dawna stanowi problem kliniczny w terapii trądziku różowatego.5 Jednym z czynników powodujących rumień są nieprawidłowe reakcje wazomotoryczne skóry, prowadzące do rozszerzenia powierzchownych naczyń krwionośnych twarzy.45 Reakcja naczyń na bodźce wazoaktywne wzbudziła zainteresowanie badaniem agonistów receptorów α2-adrenergicznych jako potencjalnych środków terapeutycznych redukujących rumień.45
Brymonidyna w postaci 0,33% żelu została zatwierdzona przez FDA w USA w sierpniu 2013 roku i przez Ministerstwo Zdrowia Kanady w lutym 2014 roku jako nowy lek do leczenia trądziku różowatego i pierwszy miejscowy preparat zatwierdzony do terapii rumienia twarzy w tej chorobie. Brymonidyna (pierwotnie stosowana jako krople do oczu w leczeniu jaskry) jest wysoce selektywnym agonistą receptorów α2-adrenergicznych o silnym działaniu wazokonstrykcyjnym.46
W badaniach wykazano, że 4-tygodniowa terapia trądziku różowatego 0,5% żelem brymonidyny, stosowanym raz dziennie, wykazywała znacznie większą skuteczność niż placebo.47 Znacząca poprawa była widoczna już po 30 minutach od pierwszego zastosowania. Działania niepożądane były umiarkowane i obejmowały rumień (5,1%), świąd (5,0%), podrażnienie skóry (1,2%) oraz nasilenie trądziku różowatego (1,1%). Nie zaobserwowano tachyfilaksji ani efektu odstawienia. Ponadto niedawno opublikowano dane z 12-miesięcznego wieloośrodkowego, otwartego badania klinicznego potwierdzające długoterminową skuteczność brymonidyny bez rozwoju tachyfilaksji w leczeniu umiarkowanego i ciężkiego rumienia w przebiegu trądziku różowatego.48
Niedawno zakończono drugą fazę badań klinicznych nad innym obiecującym agonistą receptorów α-adrenergicznych – oksymetazoliną.49 Wyniki powinny być dostępne w najbliższym czasie.
Inne metody leczenia
Miejscowy 10% sulfacetamid sodu z 5% zawartością siarki
Miejscowy 10% sulfacetamid sodu z 5% zawartością siarki jest stosowany od ponad 50 lat w leczeniu trądziku różowatego, choć mechanizm jego działania nie jest do końca poznany. W 8-tygodniowym badaniu wykazano, że sulfacetamid sodu 10% z 5% siarki znacząco zmniejszał zmiany zapalne (78% w porównaniu do 18%) oraz nasilenie rumienia twarzy (83% w porównaniu do 31%, p<0,001) w porównaniu do placebo (substancji nośnikowej preparatu).50 Jednak badania oceniające tę terapię są ograniczone i ogólnie niskiej jakości.28
Doustny izotretynoina
Doustny izotretynoina może być stosowany poza wskazaniami do leczenia ciężkich lub opornych przypadków grudkowo-krostkowego trądziku różowatego i może pomóc spowolnić lub zatrzymać progresję rhinophyma.
W 12-tygodniowym badaniu porównującym skuteczność różnych dawek izotretynoiny, doksycykliny i placebo w leczeniu trądziku różowatego izotretynoina w dawce 0,3 mg/kg wykazała skuteczność porównywalną do doksycykliny i była dobrze tolerowana.51 Jednak izotretynoina powinna być przepisywana tylko pod ścisłą kontrolą, zwłaszcza u kobiet w wieku rozrodczym, ponieważ odpowiednia strategia antykoncepcyjna jest kluczowa ze względu na jej teratogenny potencjał.
Laserowe i świetlne metody leczenia
Laserowe i świetlne metody leczenia są z powodzeniem stosowane od wielu lat w leczeniu naczyniowych objawów trądziku różowatego. W badaniach randomizowanych wykazano, że laser barwnikowy o impulsowym działaniu oraz intensywne metody światła impulsowego są równie skuteczne w redukcji rumienia i teleangiektazji u pacjentów z rumieniowo-teleangiektatycznym trądzikiem różowatym.52
Miejscowy nadtlenek benzoilu i klindamycyna
W 12-tygodniowym badaniu klinicznym53 u pacjentów z trądzikiem różowatym stosujących 5% nadtlenek benzoilu i 1% klindamycynę raz dziennie wykazano znaczną skuteczność w redukcji grudkowo-krostkowych zmian skórnych w porównaniu do placebo (71,3% vs. 19,3%, p=0,0056). Działania niepożądane były nieznacznie częstsze w grupie leczonej, a najczęściej zgłaszanymi objawami były pieczenie i świąd.
Miejscowy pimekrolimus
W niedawnym badaniu wykazano skuteczność i dobrą tolerancję 1% kremu pimekrolimusu w leczeniu trądziku różowatego.54 Działania niepożądane były krótkotrwałe i łagodne, obejmujące miejscowe pieczenie, świąd, suchość i mrowienie.
Podsumowanie
Istnieje wiele metod leczenia trądziku różowatego, jednak skuteczność tylko niektórych preparatów jest dobrze udokumentowana w badaniach naukowych. Jeśli to możliwe, decyzja terapeutyczna powinna opierać się na wysokim poziomie dowodów oraz uwzględniać takie czynniki jak podtyp trądziku różowatego, nasilenie choroby, oczekiwania pacjenta, tolerancję na leczenie, koszty oraz wcześniejszą odpowiedź na terapię.
Miejscowy kwas azelainowy i metronidazol są uważane za bezpieczne i skuteczne terapie pierwszego rzutu. Stosowanie subantybiotykowych dawek doksycykliny ma solidne podstawy naukowe i może być używane w leczeniu umiarkowanych i ciężkich postaci grudkowo-krostkowego lub ocznego trądziku różowatego. Niskie dawki izotretynoiny lub zabiegi chirurgiczne mogą być stosowane w leczeniu postaci fimatoidalnej. Terapia laserowa może być skutecznie wykorzystywana do leczenia teleangiektazji. Nowa metoda leczenia – brymonidyna – jest przeznaczona do terapii rozlanego rumienia twarzy w trądziku różowatym. Kompleksowy plan leczenia powinien również obejmować strategie niemedyczne, mające na celu poprawę jakości życia, profilaktykę zaostrzeń, odpowiednią codzienną pielęgnację skóry, terapię kamuflażu oraz ochronę przeciwsłoneczną.
Konieczne są dalsze badania nad skutecznością terapii skojarzonej, izotretynoiny, sulfacetamidu oraz nowo opracowywanych preparatów w porównaniu do standardowych metod leczenia.
Literatura:
- Crawford GH, Pelle MT, James WD. Rosacea: I. Etiology, pathogenesis, and subtype classification. J Am Acad Dermatol. 2004 Sep; 51(3):327-41; quiz 42-4.
- Powell FC. Clinical practice. Rosacea. N Engl J Med. 2005 Feb 24; 352(8):793-803.
- Wilkin J, Dahl M, Detmar M, et al. Standard grading system for rosacea: report of the National Rosacea Society Expert Committee on the classification and staging of rosacea. J Am Acad Dermatol. 2004 Jun; 50(6):907-12.
- Wilkin J, Dahl M, Detmar M, et al. Standard classification of rosacea: report of the National Rosacea Society Expert Committee on the classification and staging of rosacea. J Am Acad Dermatol. 2002 Apr; 46(4):584-7.
- Gupta AK, Chaudhry MM. Rosacea and its management: an overview. J Eur Acad Dermatol Venereol. 2005 May; 19(3):273-85.
- Jansen T, Plewig G. Rosacea: classification and treatment. J R Soc Med. 1997 Mar; 90(3):144-50.
- Tan J, Berg M. Rosacea: current state of epidemiology. J Am Acad Dermatol. 2013 Dec; 69(6 Suppl 1):S27-35.
- Gallo R, Drago F, Paolino S, et al. Rosacea treatments: What’s new and what’s on the horizon? Am J Clin Dermatol. 2010; 11(5):299-303.
- Layton A, Thiboutot D. Emerging therapies in rosacea. J Am Acad Dermatol. 2013 Dec; 69(6 Suppl 1):S57-65.
- Aksoy B, Altaykan-Hapa A, Egemen D, et al. The impact of rosacea on quality of life: effects of demographic and clinical characteristics and various treatment modalities. Br J Dermatol. 2010 Oct; 163(4):719-25.
- Wolf JE, Jr., Del Rosso JQ. The CLEAR trial: results of a large community-based study of metronidazole gel in rosacea. Cutis. 2007 Jan; 79(1):73-80.
- Gooderham M. Rosacea and its topical management. Skin Therapy Lett. 2009 Feb; 14(2):1-3.
- Nielsen PG. Treatment of rosacea with 1% metronidazole cream. A doubleblind study. Br J Dermatol. 1983 Mar; 108(3):327-32.
- Narayanan S, Hunerbein A, Getie M, et al. Scavenging properties of metronidazole on free oxygen radicals in a skin lipid model system. J Pharm Pharmacol. 2007 Aug; 59(8):1125-30.
- Dahl MV, Katz HI, Krueger GG, et al. Topical metronidazole maintains remissions of rosacea. Arch Dermatol. 1998 Jun; 134(6):679-83.
- Breneman DL, Stewart D, Hevia O, et al. A double-blind, multicenter clinical trial comparing efficacy of once-daily metronidazole 1 percent cream to vehicle in patients with rosacea. Cutis. 1998 Jan; 61(1):44-7.
- Bleicher PA, Charles JH, Sober AJ. Topical metronidazole therapy for rosacea. Arch Dermatol. 1987 May; 123(5):609-14.
- Rowe-Jones DC, Peel AL, Kingston RD, et al. Single dose cefotaxime plus metronidazole versus three dose cefuroxime plus metronidazole as prophylaxis against wound infection in colorectal surgery: multicentre prospective randomised study. BMJ. 1990 Jan 6; 300(6716):18-22.
- Yoo J, Reid DC, Kimball AB. Metronidazole in the treatment of rosacea: do formulation, dosing, and concentration matter? J Drugs Dermatol. 2006 Apr; 5(4):317-9.
- Maddin S. A comparison of topical azelaic acid 20% cream and topical metronidazole 0.75% cream in the treatment of patients with papulopustular rosacea. J Am Acad Dermatol. 1999 Jun;40(6 Pt 1):961-5.
- Dahl MV, Jarratt M, Kaplan D, et al. Once-daily topical metronidazole cream formulations in the treatment of the papules and pustules of rosacea. J Am Acad Dermatol. 2001 Nov; 45(5):723-30.
- Jorizzo JL, Lebwohl M, Tobey RE. The efficacy of metronidazole 1% cream once daily compared with metronidazole 1% cream twice daily and their vehicles in rosacea: a double-blind clinical trial. J Am Acad Dermatol. 1998 Sep; 39(3):502-4.
- Tan JK, Girard C, Krol A, et al. Randomized placebo-controlled trial of metronidazole 1% cream with sunscreen SPF 15 in treatment of rosacea. J Cutan Med Surg. 2002 Nov-Dec; 6(6):529-34.
- Fitton A, Goa KL. Azelaic acid. A review of its pharmacological properties and therapeutic efficacy in acne and hyperpigmentary skin disorders. Drugs. 1991 May; 41(5):780-98.
- Thiboutot D, Thieroff-Ekerdt R, Graupe K. Efficacy and safety of azelaic acid (15%) gel as a new treatment for papulopustular rosacea: results from two vehicle-controlled, randomized phase III studies. J Am Acad Dermatol. 2003 Jun; 48(6):836-45.
- Carmichael AJ, Marks R, Graupe KA, et al. Topical azelaic acid in the treatment of rosacea. J Dermatolog Treat. 1993; 4(suppl):S19-S22.
- Bjerke R, Fyrand O, Graupe K. Double-blind comparison of azelaic acid 20% cream and its vehicle in treatment of papulo-pustular rosacea. Acta Derm Venereol. 1999 Nov; 79(6):456-9.
- van Zuuren EJ, Kramer S, Carter B, et al. Interventions for rosacea. Cochrane Database Syst Rev. 2011(3):CD003262.
- Colon LE, Johnson LA, Gottschalk RW. Cumulative irritation potential among metronidazole gel 1%, metronidazole gel 0,75%, and azelaic acid gel 15%. Cutis. 2007 Apr; 79(4):317-21.
- Thiboutot DM, Fleischer AB, Jr., Del Rosso JQ, et al. Azelaic acid 15% gel once daily versus twice daily in papulopustular rosacea. J Drugs Dermatol. 2008 Jun; 7(6):541-6.
- Pelle MT, Crawford GH, James WD. Rosacea: II. Therapy. J Am Acad Dermatol. 2004 Oct; 51(4):499-512; quiz 3-4.
- Maibach H. Second-generation tetracyclines, a dermatologic overview: clinical uses and pharmacology. Cutis. 1991 Nov; 48(5):411-7.
- Del Rosso JQ, Webster GF, Jackson M, et al. Two randomized phase III clinical trials evaluating anti-inflammatory dose doxycycline (40-mg doxycycline, USP capsules) administered once daily for treatment of rosacea. J Am Acad Dermatol. 2007 May; 56(5):791-802.
- Del Rosso JQ, Schlessinger J, Werschler P. Comparison of anti-inflammatory dose doxycycline versus doxycycline 100 mg in the treatment of rosacea. J Drugs Dermatol. 2008 Jun; 7(6):573-6.
- Smith K, Leyden JJ. Safety of doxycycline and minocycline: a systematic review. Clin Ther. 2005 Sep; 27(9):1329-42.
- Sanchez J, Somolinos AL, Almodovar PI, et al. A randomized, double-blind, placebo-controlled trial of the combined effect of doxycycline hyclate 20-mg tablets and metronidazole 0.75% topical lotion in the treatment of rosacea. J Am Acad Dermatol. 2005 Nov; 53(5):791-7.
- Lacey N, Delaney S, Kavanagh K, et al. Mite-related bacterial antigens stimulate inflammatory cells in rosacea. Br J Dermatol. 2007 Sep; 157(3): 474-81.
- O’Reilly N, Menezes N, Kavanagh K. Positive correlation between serum immunoreactivity to Demodex-associated Bacillus proteins and erythematotelangiectatic rosacea. Br J Dermatol. 2012 Nov; 167(5):1032-6.
- Allen KJ, Davis CL, Billings SD, et al. Recalcitrant papulopustular rosacea in an immunocompetent patient responding to combination therapy with oral ivermectin and topical permethrin. Cutis. 2007 Aug; 80(2):149-51.
- Forstinger C, Kittler H, Binder M. Treatment of rosacea-like demodicidosis with oral ivermectin and topical permethrin cream. J Am Acad Dermatol. 1999 Nov; 41(5 Pt 1):775-7.
- Karincaoglu Y, Bayram N, Aycan O, et al. The clinical importance of demodex folliculorum presenting with nonspecific facial signs and symptoms. J Dermatol. 2004 Aug; 31(8):618-26.
- Galderma. Randomized, double-blind, parallel-group, vehicle-controlled, dose-finding study investigating the pharmacodynamics and safety of three concentrations of CD07805/47 topical gel (0,07%, 0,18%, and 0,50%), applied in subjects with moderate to severe erythematotelangiectatic rosacea. In: ClinicalTrials.gov, Identifier: NCT00989014. Last updated September 19, 2013. Available at: http://clinicaltrials.gov/ct2/show/NCT00989014. Accessed: March 9, 2014.
- Galderma. A phase 3 randomized, double blind, 12 week vehicle controlled, parallel group study assessing the efficacy and safety of CD5024 1% cream versus vehicle cream in subjects with papulopustular rosacea, followed by a 40 week investigator blinded extension comparing the long term safety of CD5024 1% cream versus azelaic Acid 15% gel. In: ClinicalTials.gov, Identifier: NCT01493687. Last updated January 27, 2014. Available at: http://clinicaltrials.gov/ct2/show/NCT01493687?term=NCT01493687&rank=1. Accessed: March 10, 2014.
- Galderma. Efficacy and safety of CD5024 1% cream versus metronidazole 0.75% cream in subjects with papulopustular rosacea over 16 weeks treatment, followed by a 36-week extension period (ATTRACT).In: ClinicalTrials.gov, Identifier: NCT01493947. Last updated December 20, 2013. Available at: http://clinicaltrials.gov/ct2/show/NCT01493947?term=NCT01493947&rank=1. Accessed: March 9, 2014.
- Del Rosso JQ. Advances in understanding and managing rosacea: part 2: the central role, evaluation, and medical management of diffuse and persistent facial erythema of rosacea. J Clin Aesthet Dermatol. 2012 Mar; 5(3):26-36.
- Rahman MQ, Ramaesh K, Montgomery DM. Brimonidine for glaucoma. Expert Opin Drug Saf. 2010 May; 9(3):483-91.
- Fowler J. Jr., Jackson M, Moore A, et al. Efficacy and safety of once-daily topical brimonidine tartrate gel 0.5% for the treatment of moderate to severe facial erythema of rosacea: results of two randomized, double-blind, and vehiclecontrolled pivotal studies. J Drugs Dermatol. 2013 Jun 1; 12(6):650-6.
- Moore A, Kempers S, Murakawa G, et al. Long-term safety and efficacy of once-daily topical brimonidine tartrate gel 0.5% for the treatment of moderate to severe facial erythema of rosacea: results of a 1-year open-label study. J Drugs Dermatol. 2014 Jan; 13(1):56-61.
- Allergan. Safety and tolerability of AGN-199201 in patients with erythema associated with rosacea. In: Clinical Trials.gov, Identifier: NCT01579084. Last updated September 12, 2013. Available at: http://clinicaltrials.gov/ct2/show/NCT01579084?term=NCT01579084&rank=1. Accessed: March 10, 2014.
- Sauder DN, Miller R, Gratton D, et al. The treatment of rosacea: the safety and efficacy of sodium sulfacetamide 10% and sulfur 5% lotion (Novacet) is demonstrated in a double-blind study. J Dermatolog Treat. 1997; 8(2):79-85.
- Gollnick H, Blume-Peytavi U, Szabo EL, et al. Systemic isotretinoin in the treatment of rosacea – doxycycline- and placebo-controlled, randomized clinical study. J Dtsch Dermatol Ges. 2010 Jul; 8(7):505-15.
- Neuhaus IM, Zane LT, Tope WD. Comparative efficacy of nonpurpuragenic pulsed dye laser and intense pulsed light for erythematotelangiectatic rosacea. Dermatol Surg. 2009 Jun; 35(6):920-8.
- Breneman D, Savin R, VandePol C, et al. Double-blind, randomized, vehiclecontrolled clinical trial of once-daily benzoyl peroxide/clindamycin topical gel in the treatment of patients with moderate to severe rosacea. Int J Dermatol. 2004 May; 43(5):381-7.
- Kim MB, Kim GW, Park HJ, et al. Pimecrolimus 1% cream for the treatment of rosacea. J Dermatol. 2011 Dec; 38(12):1135-9.
CHANG B., KURYAN A. – Uniwersytet Alberta, Edmonton (Kanada)
BARANKIN B. – Centrum Dermatologiczne Toronto (Kanada)