Leczenie trądziku w czasie ciąży
Trądzik pospolity (acne vulgaris) to przewlekła choroba zapalna jednostki włosowo-łojowej, charakteryzująca się zmianami niezapalnymi (zaskórniki) oraz zapalnymi (grudki, krosty i guzki), które mogą prowadzić do powstawania blizn i stresu psychicznego. U kobiet planujących ciążę lub będących już w okresie ciąży, schorzenie to może być szczególnie uciążliwe ze względu na fizjologiczne zmiany oraz nieprzewidywalny przebieg trądziku w tym okresie. U wielu kobiet z trądzikiem obserwuje się poprawę w pierwszym trymestrze ciąży, jednak w trzecim trymestrze możliwe jest jego nasilenie, co jest związane ze wzrostem poziomu androgenów i zwiększoną produkcją łoju. Oprócz zmian hormonalnych, wpływ mogą mieć również zmiany immunologiczne towarzyszące ciąży. Zmiany zapalne mają tendencję do bycia częstszymi niż niezapalne i często obejmują tułów. Pacjentki z trądzikiem w wywiadzie są bardziej podatne na jego rozwój podczas ciąży.
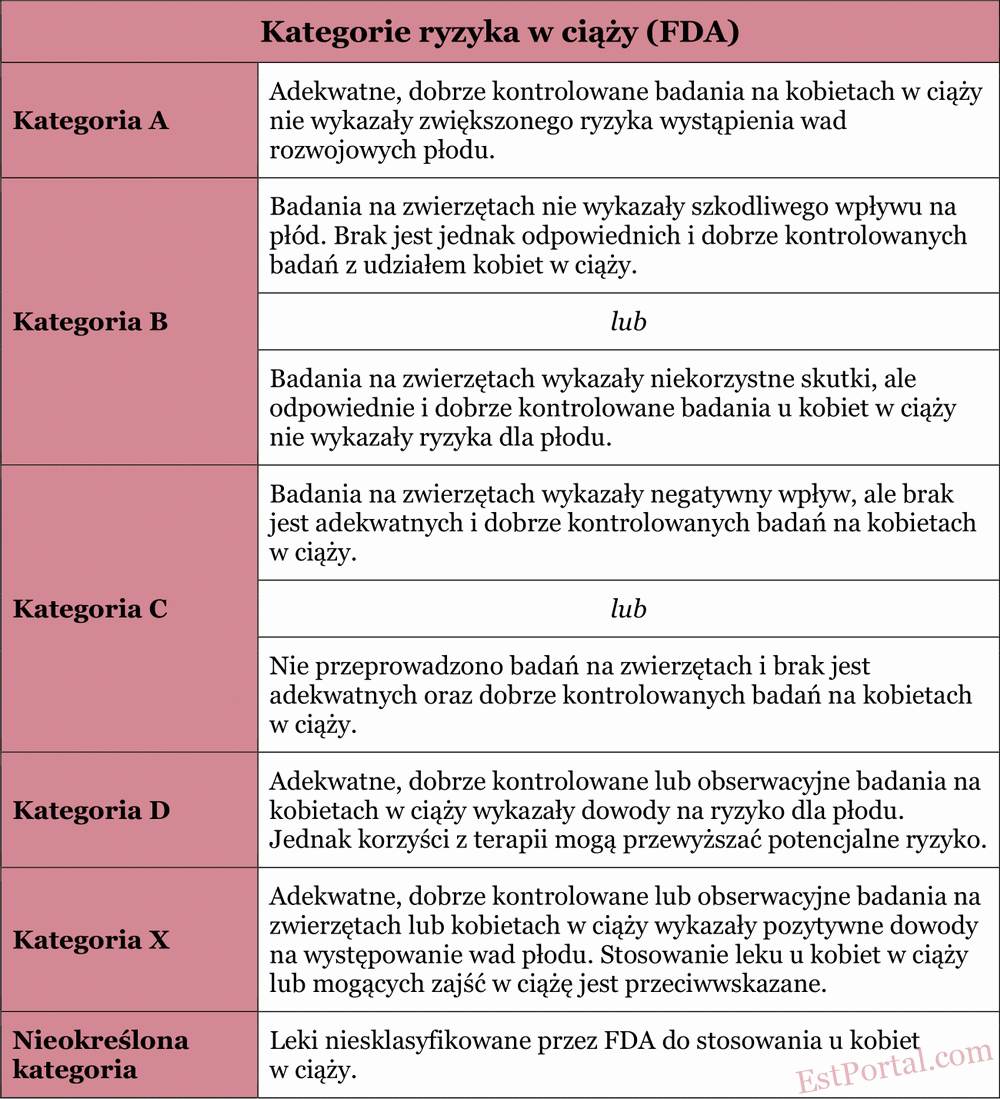
Leczenie trądziku u kobiet w ciąży może być trudne, ponieważ wiele skutecznych i powszechnie stosowanych terapii jest przeciwwskazanych lub niezalecanych. Dlatego dla lekarza niezwykle istotne jest uwzględnienie ograniczeń w leczeniu w okresie ciąży, określonych przez Amerykańską Agencję ds. Żywności i Leków (FDA) [patrz: tabela 1].
Tabela 1
Ze względu na istniejące problemy etyczne, uniemożliwiające przeprowadzanie badań klinicznych w czasie ciąży, dane farmakokinetyczne i farmakodynamiczne dotyczące oceny bezpieczeństwa leków w tym okresie są ograniczone, a randomizowane kontrolowane badania dotyczące leków przeciwtrądzikowych nie istnieją. W związku z tym zalecenia dotyczące terapii w czasie ciąży opierają się głównie na badaniach obserwacyjnych oraz danych przedklinicznych uzyskanych na modelach zwierzęcych.
W niniejszym przeglądzie omówimy dostępne dane dotyczące bezpieczeństwa i skuteczności powszechnie stosowanych leków przeciwtrądzikowych oraz przedstawimy praktyczne podejście do leczenia trądziku w czasie ciąży w oparciu o najnowsze dostępne informacje [zob. tabela 2]. Dzięki tym informacjom lekarze będą mogli opracować bezpieczny i skuteczny schemat leczenia trądziku dla tej wyjątkowej grupy pacjentek.
Tabela 2
Wyszukiwanie literatury i źródła danych
Na potrzeby tego przeglądu przeprowadzono wyszukiwanie w bazie PubMed, używając następujących słów kluczowych:
- trądzik;
- ciąża;
- kwas azelainowy;
- nadtlenek benzoilu;
- kwas salicylowy;
- kwas aminolewulinowy;
- terapia fotodynamiczna;
- FDA ciąża.
Nie stosowano ograniczeń co do daty publikacji. Do wyszukiwania włączono metaanalizy randomizowanych badań kontrolowanych, badania kliniczne i przeglądy literatury. Dodatkowo przeszukano bazy danych EMBASE, Cochrane oraz UpToDate.
Leczenie miejscowe
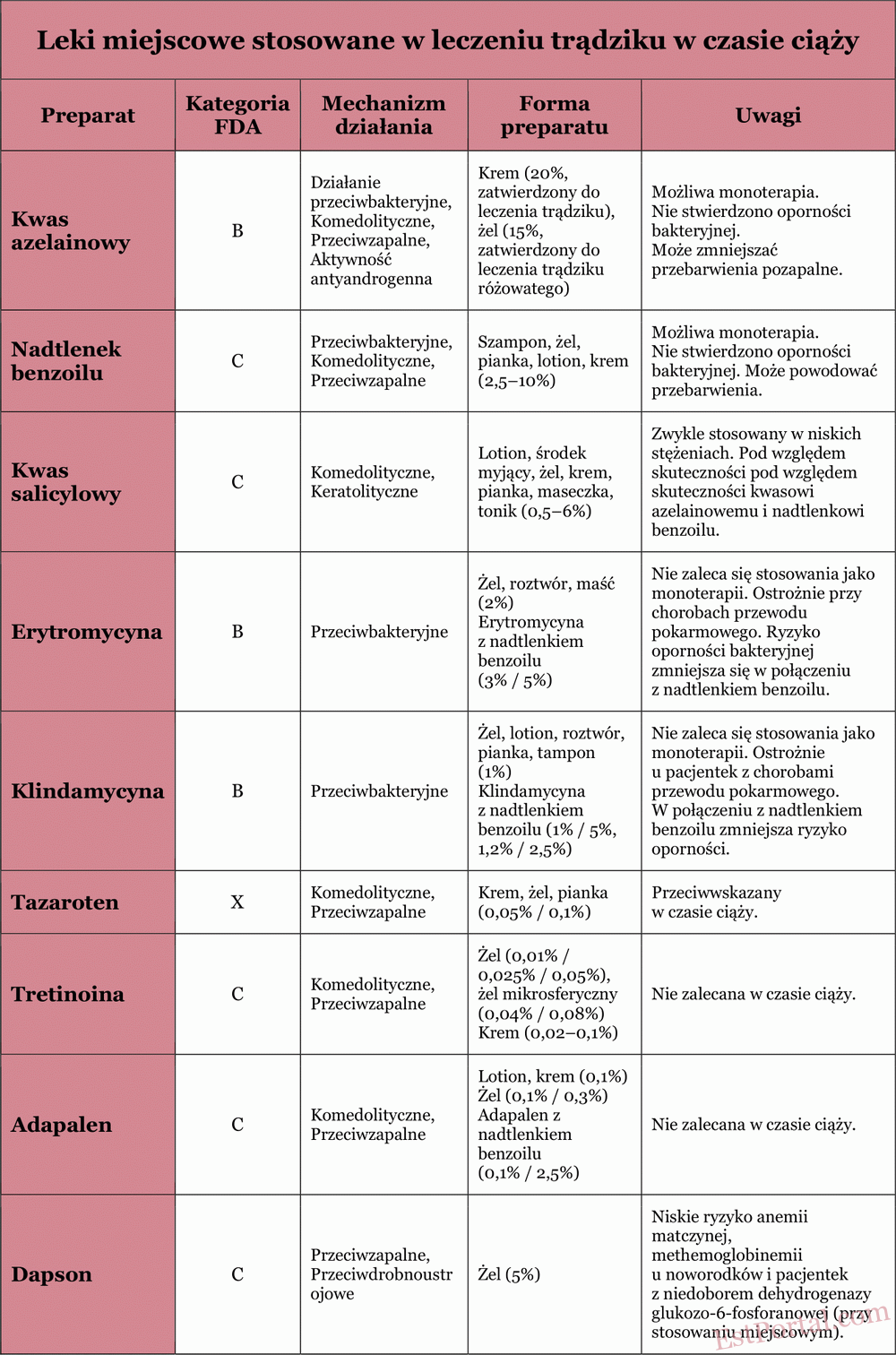
W przypadku łagodnego lub umiarkowanego trądziku leczenie miejscowe jest standardową metodą terapeutyczną. Stanowi ono również istotny element leczenia cięższych postaci trądziku i działa synergistycznie z lekami doustnymi. W czasie ciąży należy szczególnie uwzględнити stopień ogólnoustrojowego wchłaniania miejscowych preparatów przeciwtrądzikowych. Właściwości najczęściej stosowanych środków miejscowych opisano w kolejnych sekcjach oraz zestawiono w tabeli 3.
Tabela 3
Kwas azelainowy
Kwas azelainowy jest klasyfikowany jako lek kategorii B w czasie ciąży, ponieważ badania na zwierzętach nie wykazały działania teratogennego, a dane z badań na ludziach są niedostępne. Kwas azelainowy to naturalnie występujący kwas dikarboksylowy o właściwościach przeciwbakteryjnych, komedolitycznych i łagodnie przeciwzapalnych, z dodatkową zaletą w postaci redukcji pozapalnej hiperpigmentacji. Nie stwierdzono oporności P. acnes na kwas azelainowy. Około 4% preparatu wchłania się do krwiobiegu po aplikacji na skórę.
Nadtlenek benzoilu
Nadtlenek benzoilu jest klasyfikowany jako lek kategorii C w czasie ciąży. Około 5% wchłania się do krwiobiegu i jest całkowicie metabolizowany do kwasu benzoesowego, który znany jest również jako dodatek do żywności. Dzięki szybkiemu klirensowi nerkowemu nie oczekuje się toksyczności ogólnoustrojowej, a ryzyko wad wrodzonych u płodu uważane jest za teoretycznie niskie. Nadtlenek benzoilu ma działanie przeciwbakteryjne, komedolityczne i przeciwzapalne. Do tej pory nie odnotowano oporności P. acnes na nadtlenek benzoilu. Uznawany jest za bezpieczny w czasie ciąży i pomaga zapobiegać rozwojowi oporności na antybiotyki, gdy jest stosowany w połączeniu z nimi.
Kwas salicylowy
Kwas salicylowy jest klasyfikowany jako lek kategorii C w czasie ciąży. Nie ma badań dotyczących stosowania miejscowego kwasu salicylowego u ludzi w okresie ciąży, choć opisano wady rozwojowe u zarodków szczurów po ogólnoustrojowym narażeniu na kwas salicylowy oraz po podaniu aspiryny w ciąży. Jest to środek keratolityczny. Stosowanie wysokich stężeń kwasu salicylowego w leczeniu hiperkeratozy skóry wiązało się z przypadkami toksyczności salicylanów, jednak nie są znane podobne przypadki w związku ze stosowaniem tego składnika w terapii trądziku. Ryzyko w czasie ciąży uważa się za niskie, jeśli stosuje się go miejscowo na ograniczonych obszarach skóry i przez krótki czas.
Antybiotyki miejscowe
Antybiotyki miejscowe od dawna są stosowane w leczeniu trądziku zapalnego. Erytromycyna i klindamycyna to dwa najczęściej przepisywane antybiotyki na trądzik u kobiet w ciąży. Oba należą do kategorii B w ciąży. Krótkotrwałe miejscowe stosowanie erytromycyny i klindamycyny uważa się za bezpieczne podczas ciąży. Jednak skutki ich długotrwałego stosowania nie zostały zbadane. Z uwagi na doniesienia o przypadkach rzekomobłoniastego zapalenia jelita grubego wywołanego przez Clostridium, klindamycynę miejscową należy stosować ostrożnie u pacjentek z chorobami przewodu pokarmowego w wywiadzie. Klindamycyna i erytromycyna stosowane miejscowo zmniejszają liczbę P. acnes w mieszkach łojowych poprzez hamowanie syntezy białek bakteryjnych, tym samym redukując stan zapalny. Połączenie miejscowych antybiotyków z nadtlenkiem benzoilu zmniejsza ryzyko oporności i zwiększa skuteczność leczenia.
Retinoidy miejscowe
Retinoidy miejscowe są pochodnymi witaminy A i są stosowane w leczeniu trądziku od ponad 30 lat. W Stanach Zjednoczonych należą do nich adapalen, tretynoina i tazaroten. Adapalen i tretynoina są klasyfikowane przez FDA jako kategoria C w ciąży, natomiast tazaroten jest zakwalifikowany do kategorii X. Jest to częściowo związane z często występującymi wadami wrodzonymi po stosowaniu ogólnoustrojowego retinoidu — izotretynoiny. Dlatego tazaroten nie jest zalecany do stosowania w czasie ciąży.
Pomimo doniesień o możliwych wadach wrodzonych, miejscowe adapalen i tretynoina raczej nie prowadzą do takich zaburzeń, biorąc pod uwagę ich słabe wchłanianie przez skórę. Niedawno przeprowadzona metaanaliza wykluczyła istotne zwiększenie ryzyka poronień, wad wrodzonych, przedwczesnych porodów czy niskiej masy urodzeniowej. Mechanizmy ich działania obejmują przyspieszenie różnicowania keratynocytów, działanie komedolityczne i przeciwzapalne. Niemniej jednak, nie są one zalecane w ciąży, ponieważ stosunek ryzyka do korzyści pozostaje niepewny.
Dapson miejscowy
Dapson miejscowy jest syntetycznym sulfonem o właściwościach przeciwbakteryjnych i przeciwzapalnych. W czasie ciąży jest klasyfikowany jako lek kategorii C. Wysokie dawki w badaniach na zwierzętach nie wykazały działania teratogennego. Dotychczasowe dane nie wskazują, aby stosowanie dapsonu miejscowego w ciąży wiązało się ze zwiększonym ryzykiem wad wrodzonych u płodu. Ryzyko wystąpienia anemii u matki, a także hiperbilirubinemii i niedokrwistości hemolitycznej u noworodków, opisywano przy doustnym stosowaniu dapsonu u pacjentów z niedoborem dehydrogenazy glukozo-6-fosforanowej, jednak przy stosowaniu miejscowym ryzyko to jest niskie.
Dapson miejscowy został zatwierdzony do leczenia trądziku w 2005 roku. Należy zachować ostrożność ze względu na jego stosunkowo niedawną obecność na rynku oraz brak kontrolowanych badań potwierdzających jego bezpieczeństwo w czasie ciąży. Dapson może być stosowany miejscowo u kobiet w ciąży, jednak jego bezpieczeństwo nie zostało jednoznacznie potwierdzone. Stosowanie powinno być rozważane wyłącznie wtedy, gdy potencjalne korzyści przeważają nad możliwym ryzykiem.
Leki doustne
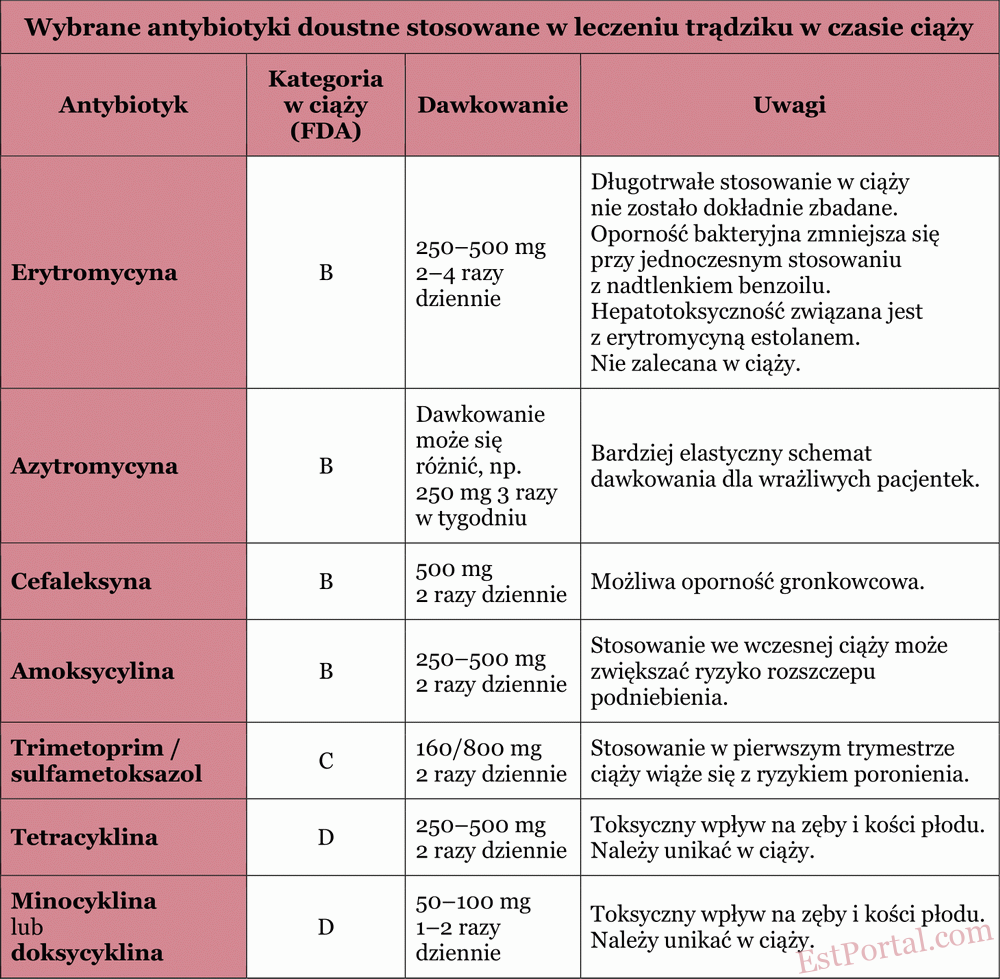
Niektórzy pacjenci nie osiągają zadowalających rezultatów, stosując jedynie leczenie miejscowe. Leki doustne są przede wszystkim zalecane pacjentom z umiarkowaną i ciężką postacią trądziku zapalnego, a także w przypadkach nieskuteczności terapii miejscowej. Właściwości najczęściej stosowanych leków doustnych opisano w kolejnych sekcjach oraz w tabeli 4.
Tabela 4
Antybiotyki doustne
Antybiotyki doustne poprawiają przebieg trądziku zapalnego poprzez hamowanie wzrostu P. acnes w jednostce łojowo-włosowej. Antybiotyki z grupy tetracyklin (w tym doksycyklina i minocyklina) wykazują nie tylko działanie przeciwbakteryjne, але również bezpośrednie działanie przeciwzapalne. Najczęściej stosowanymi antybiotykami (z wyłączeniem kobiet w ciąży) są:
- Doksycyklina;
- Minocyklina;
- Erytromycyna;
- Azytromycyna;
- Cefaleksyna;
- Trimetoprim/Sulfametoksazol.
Ze względu na rosnącą oporność bakteryjną zaleca się łączenie miejscowego nadtlenku benzoilu z antybiotykami doustnymi, ograniczenie ich stosowania do krótkich kursów oraz unikanie używania antybiotyków doustnych jako terapii podtrzymującej trądzik. Aby ograniczyć rozwój oporności, należy również unikać częstych zmian antybiotyków; jeśli dany antybiotyk był wcześniej skuteczny, należy go zastosować ponownie. Antybiotyki doustne powinny być stosowane u kobiet w ciąży wyłącznie wtedy, gdy ich potrzeba jest jasno uzasadniona.
Erytromycyna jest makrolidem zaliczanym do kategorii B w czasie ciąży. Lek słabo przenika przez łożysko, co skutkuje niskim stężeniem w tkankach płodu. Erytromycyna jest ogólnie uznawana za bezpieczną na każdym etapie ciąży, jeśli stosowana jest przez kilka tygodni. Może być uznawana za antybiotyk z wyboru w leczeniu ciężkich zapalnych postaci trądziku u kobiet w ciąży. Jednakże jej długotrwałe stosowanie (ponad 6 tygodni) nie było dokładnie przebadane. Należy zaznaczyć, że estolan erytromycyny jest przeciwwskazany z powodu hepatotoksyczności u matki.
Azytromycyna to kolejny makrolid, który FDA zalicza do kategorii B w czasie ciąży. Badania na zwierzętach wykazały, że azytromycyna przenika przez łożysko, nie powodując negatywnych skutków dla płodu. Azytromycyna jest uznawana za akceptowalną u kobiet w ciąży z trądzikiem, chociaż dostępnych danych dotyczących jej bezpieczeństwa jest mniej niż w przypadku erytromycyny.
Amoksycylina została zaklasyfikowana przez FDA do kategorii B w czasie ciąży. Jej stosowanie we wczesnym okresie ciąży może zwiększać ryzyko rozszczepu podniebienia. Amoksycylina może być stosowana samodzielnie lub w połączeniu z innymi lekami jako lek z wyboru w leczeniu opornego trądziku. Może powodować działania niepożądane ze strony przewodu pokarmowego, takie jak nudności i wymioty.
Cefaleksyna to cefalosporyna pierwszej generacji o właściwościach przeciwzapalnych, zaliczana do kategorii B w czasie ciąży. W badaniach na zwierzętach nie wykazano związku cefaleksyny z wadami rozwojowymi zarodka. Chociaż jest skuteczna w leczeniu trądziku, istnieją pewne obawy dotyczące rozwoju oporności gronkowców na ten antybiotyk.
Trimetoprim działa jako antagonista kwasu foliowego i jest sklasyfikowany jako lek kategorii C w czasie ciąży. Ostatnie badania wykazały, że stosowanie trimetoprimu w pierwszym trymestrze było związane z podwojeniem ryzyka poronienia. Dlatego stosowanie trimetoprimu/sulfametoksazolu w czasie ciąży zalecane jest wyłącznie wtedy, gdy brak jest alternatywy, a korzyści przeważają nad ryzykiem.
Tetracykliny są klasyfikowane jako leki kategorii D w czasie ciąży. Badania na zwierzętach wykazały dowody na toksyczność embrionalną i płodową, w tym toksyczne działanie na zęby i kości płodu. Tetracykliny wiążą się z ortofosforanem wapnia i dlatego aktywnie odkładają się w zębach i kościach. Złogi leku w zębach utrzymują się przez długi czas, co powoduje żółte zabarwienie zębów mlecznych u dzieci narażonych na działanie leku po 20. tygodniu ciąży, które z czasem ciemnieją. Odkładanie się leku w kościach prowadzi do odwracalnego zahamowania wzrostu płodu i zahamowania wzrostu kości strzałkowej, szczególnie przy długotrwałym stosowaniu. Tetracyklin należy unikać w czasie ciąży, zwłaszcza po pierwszym trymestrze.
Warto zauważyć, że potrzebne są dodatkowe dowody dotyczące zalecanego czasu trwania tego rodzaju terapii. Skutki długotrwałego stosowania tych antybiotyków na płód nie są znane. Należy je rozważyć w kontekście ciężkości trądziku oraz dostępnych alternatywnych metod leczenia miejscowego. Stosowanie antybiotyków ogólnoustrojowych powinno być ograniczone do drugiego i trzeciego trymestru, po zakończeniu organogenezy, z ograniczeniem czasu leczenia do 4–6 tygodni.
Doustne kortykosteroidy
Ciężkie postacie trądziku, oporne na terapię antybiotykową, mogą ulec znacznej poprawie przy zastosowaniu doustnych kortykosteroidów. Zgodnie z klasyfikacją FDA prednizon został zakwalifikowany do kategorii C w czasie ciąży. W badaniach na zwierzętach wykazano związek między lekiem a rozszczepem podniebienia, spowolnieniem rozwoju mózgu, zmniejszoną mielinizacją i obwodem głowy. U ludzi stwierdzono zwiększone ryzyko rozszczepu podniebienia oraz niewielki wzrost częstości poronień i przedwczesnych porodów. Istnieje niewiele danych na temat zdolności steroidów systemowych i miejscowych do przenikania przez barierę łożyskową, chociaż wykazano, że miejscowe steroidy mogą wywoływać działanie ogólnoustrojowe.
Prednizon powinien być przepisywany wyłącznie w wyjątkowych przypadkach — w przypadku ciężkiego, piorunującego trądziku po pierwszym trymestrze, w minimalnych dawkach i przez ograniczony czas (nie dłużej niż 1 miesiąc). Zastosowanie steroidów w postaci niewielkiej liczby iniekcji lub krótkich kursów doustnych steroidów w rzadkich, szybko postępujących przypadkach trądziku pospolitego prawdopodobnie nie stanowi dodatkowego ryzyka dla płodu. Dawka prednizonu nie powinna przekraczać 20 mg dziennie, a czas trwania terapii — jednego miesiąca w późnych etapach ciąży.
Retinoidy doustne
Izotretynoina jest często przepisywana pacjentom (z wyjątkiem kobiet w ciąży) z uporczywym, konglobatowym trądzikiem pospolitym. Teratogenne działanie izotretynoiny jest dobrze znane, a lek ten został zakwalifikowany do kategorii X. Izotretynoina powoduje charakterystyczne wady wrodzone związane z obszarem czaszkowo-twarzowym, ośrodkowym układem nerwowym, układem sercowo-naczyniowym, grasicą i przytarczycami. Została zatwierdzona w 1982 roku i działa poprzez zmniejszenie produkcji sebum oraz normalizację procesu rogowacenia. Izotretynoina jest absolutnie przeciwwskazana w czasie ciąży.
Cynk
Cynk stanowi dodatkową opcję terapeutyczną dla kobiet w ciąży z trądzikiem. Siarczan cynku został sklasyfikowany jako lek kategorii C w ciąży, natomiast glukonian cynku nie został oficjalnie sklasyfikowany. Badania na zwierzętach i ludziach, w tym kobietach w ciąży leczonych na trądzik, nie wykazały zwiększonego ryzyka wad płodu ani uszkodzeń przy dawkach poniżej 75 mg/dzień. Cynk ma właściwości antybakteryjne, przeciwzapalne i zmniejsza produkcję sebum. Wykazano jego skuteczność w leczeniu łagodnego i umiarkowanego zapalnego trądziku jako monoterapia lub w połączeniu z innymi preparatami. Zalecana dzienna dawka cynku w czasie ciąży wynosi 11 mg/dzień. Potencjalne działania niepożądane obejmują nudności i wymioty, zazwyczaj zależne od dawki.
Terapia dodatkowa
Kwas glikolowy
Kwas glikolowy zaliczany jest do kategorii N, co oznacza, że nie został sklasyfikowany pod względem bezpieczeństwa w ciąży i stosuje się go miejscowo w leczeniu trądziku. Nie ma opublikowanych danych o niepożądanych skutkach jego stosowania podczas ciąży. Badania wykazały poprawę w przypadku zmian zapalnych i zaskórników, chociaż zaskórniki zamknięte mogą reagować wolniej. Kwas glikolowy ma również dodatkowe zalety — покращує stan шкіри після запалення та підвищує абсорбцію топічних засобів.
Terapia fotodynamiczna
Terapia fotodynamiczna została zakwalifikowana do kategorii C, a brak badań na zwierzętach oceniających jej wpływ na funkcje rozrodcze. W porównaniu z leczeniem kontrolnym, terapia fotodynamiczna wykazała istotną statystycznie poprawę nasilenia trądziku, a także trwałe rezultaty do 20. tygodnia ciąży po wielokrotnych sesjach. Brak refundacji i częstotliwość zabiegów w gabinecie dermatologicznym mogą ograniczać jej zastosowanie u kobiet w ciąży.
Wnioski
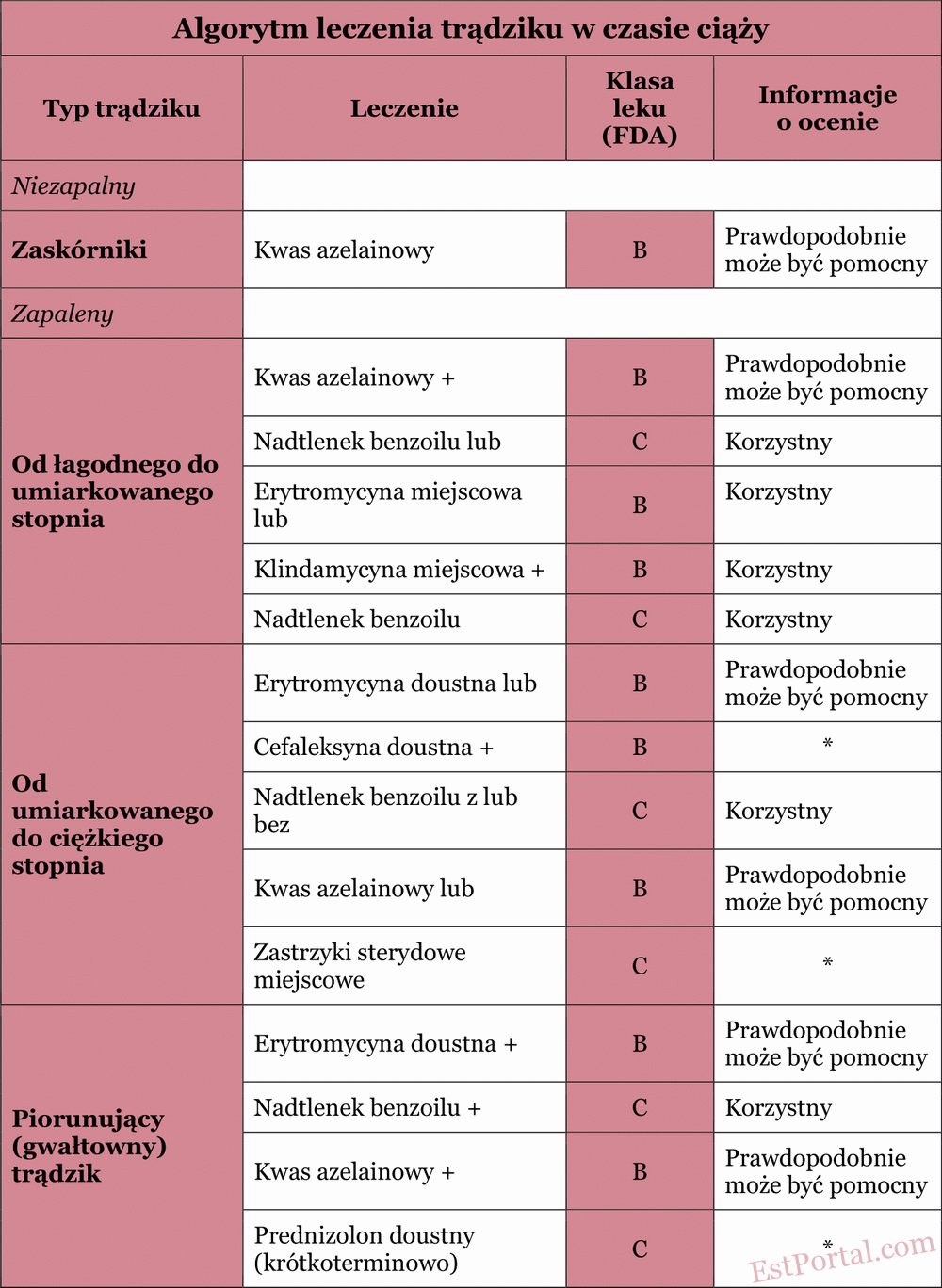
W niniejszym przeglądzie przedstawiliśmy różnorodne możliwości terapeutyczne dla lekarzy prowadzących leczenie trądziku u kobiet w ciąży. Poniżej znajduje się uproszczony algorytm, który może służyć jako punkt wyjścia przy wyborze terapii trądziku u ciężarnych.
W przypadku łagodnego trądziku, charakteryzującego się głównie niezapalnymi zmianami skórnymi, można zalecić stosowanie miejscowego preparatu z kwasem azelainowym lub nadtlenkiem benzoilu jako terapii podstawowej.
W trądziku zapalnym zaleca się rozpoczęcie leczenia od połączenia miejscowego erytromycyny lub klindamycyny z nadtlenkiem benzoilu.
W umiarkowanym i ciężkim trądziku zapalnym można rozważyć podanie doustnej erytromycyny lub cefaleksyny, które uznawane są za bezpieczne, jeśli są stosowane tylko przez kilka tygodni.
Kuracja prednizonem trwająca nie dłużej niż miesiąc może być pomocna w leczeniu błyskawicznie postępującego trądziku skupionego torbielowatego po pierwszym trymestrze. Zazwyczaj miejscowe i doustne antybiotyki nie powinny być stosowane jako monoterapia — w celu ograniczenia oporności bakteryjnej należy je łączyć z miejscowym nadtlenkiem benzoilu.
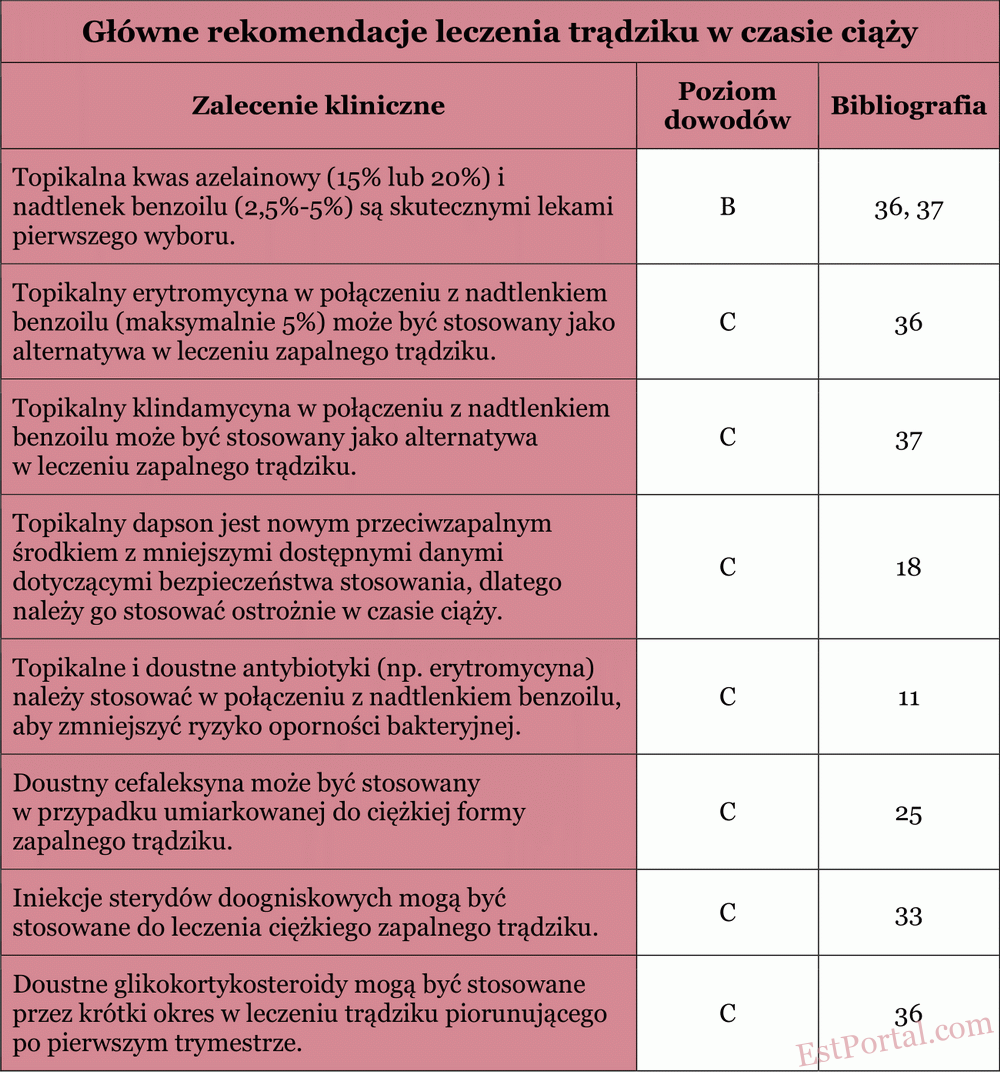
Terapie dodatkowe omówione w tym przeglądzie należy rozważać z uwzględnieniem reakcji pacjentki i jej preferencji. Główne zalecenia przedstawiono w tabeli 5. Mamy nadzieję, że niniejszy przegląd okaże się pomocny dla lekarzy leczących trądzik u kobiet w ciąży.
Tabela 5
Przedstawione dane mogą służyć jako wskazówka kliniczna przy wyborze bezpiecznej i skutecznej terapii trądziku u ciężarnych, z uwzględnieniem etapu ciąży, nasilenia objawów oraz indywidualnych cech pacjentki.
Bibliografia:
- Akhavan A, Bershad S. Topical acne drugs: review of clinical properties, systemic exposure, and safety. Am J Clin Dermatol 2003;4:473–92. CrossRef PubMed Web of Science Google Scholar
- Jones SV, Ambros-Rudolph C, Nelson-Piercy C. Skin disease in pregnancy. BMJ 2014;348:g3489. FREE Full Text Google Scholar
- Pugashetti R, Shinkai K. Treatment of acne vulgaris in pregnant patients. Dermatol Ther 2013;26:302–11. PubMed Google Scholar
- Dréno B, Blouin E, Moyse D, Bodokh I, Knol A, Khammari A. Acne in pregnant women: a French Acta Derm Venereol 2014;94:82–3. PubMed Google Scholar
- Wolverton SE, ed. Comprehensive dermatologic drug therapy. 3rd ed. Philadelphia: Saunders; 2012. Google Scholar
- Murase JE, Heller MM, Butler DC. Safety of dermatologic medications in pregnancy and lactation: part I. Pregnancy. J Am Acad Dermatol 2014;70:401.e1–14; quiz 415. Google Scholar
- Williams HC, Dellavalle RP, Garner S. Acne vulgaris. Lancet 2012;379:361–72. CrossRef PubMed Web of Science Google Scholar
- Parry MF, Rha CK. Pseudomembranous colitis caused by topical clindamycin phosphate. Arch Dermatol 1986;122:583–4. CrossRef PubMed Web of Science Google Scholar
- Siegle RJ, Fekety R, Sarbone PD, Finch RN, Deery HG, Voorhees JJ. Effects of topical clindamycin on intestinal microflora in patients with acne. J Am Acad Dermatol 1986;15(2 Pt 1):180–5. PubMed Web of Science Google Scholar
- Patel M, Bowe WP, Heughebaert C, Shalita AR. The development of antimicrobial resistance due to the antibiotic treatment of acne vulgaris: a review. J Drugs Dermatol 2010;9:655–64. PubMed Web of Science Google Scholar
- Kinney MA, Yentzer BA, Fleischer AB, Feldman SR. Trends in the treatment of acne vulgaris: are measures being taken to avoid antimicrobial resistance? J Drugs Dermatol 2010;9:519–24. PubMed Google Scholar
- Berard A, Azoulay L, Koren G, Blais L, Perreault S, Oraichi D. Isotretinoin, pregnancies, abortions and birth defects: a population-based perspective. Br J Clin Pharmacol 2007;63:196–205. CrossRef PubMed Web of Science Google Scholar
- Panchaud A, Csajka C, Merlob P. Pregnancy outcome following exposure to topical retinoids: prospective study. J Clin Pharmacol 2012;52:1844–51. CrossRef PubMed Google Scholar
- Kaplan YC, Ozsarfati J, Etwel F, Nickel , Nulman I, Koren G. Pregnancy outcomes following first trimester exposure to topical retinoids : a systematic review and meta-analysis. Br J Dermatol 2015;173:1132–41. PubMed Google Scholar
- Gamble R, Dunn J, Dawson A, et al. Topical antimicrobial treatment of acne vulgaris: an evidence-based review. Am J Clin Dermatol 2012;13:141–52. CrossRef PubMed Google Scholar
- Nosten F, McGready R, d'Alessandro U, et al. Antimalarial drugs in pregnancy: a review. Curr Drug Saf 2006;1:1–15. CrossRef PubMed Google Scholar
- James KA, Burkhart CN, Morrell DS. Emerging drugs for acne. Expert Opin Emerg Drugs 2009;14:649–59. PubMed Google Scholar
- Kong YL, Tey HL. Treatment of acne vulgaris during pregnancy and lactation. Drugs 2013;73:779–87. PubMed Google Scholar
- Thiboutot D, Gollnick H, Bettoli V, et al. New insights into the management of acne: an update from the Global Alliance to Improve Outcomes in Acne Group. J Am Acad Dermatol 2009;60(5 Suppl):S1–50. CrossRef PubMed Web of Science Google Scholar
- Romoren M, Lindbaek M, Nordeng H. Pregnancy outcome after gestational exposure to erythromycin-a population-based register study from Norway. Br J Clin Pharmacol 2012;74:1053–62. CrossRef PubMed Google Scholar
- Al Hammadi A, Al-Haddab M, Sasseville D. Dermatologic treatment during pregnancy: practical overview. J Cutan Med Surg 2006;10:183–92. Google Scholar
- Hale EK, Pomeranz MK. Dermatologic agents during pregnancy and lactation: an update and clinical review. Int J Dermatol 2002;41:197–203. CrossRef PubMed Web of Science Google Scholar
- Lin KJ, Mitchell AA, Yau W-P, Louik C, Hernández-Díaz S. Maternal exposure to amoxicillin and the risk of oral clefts. Epidemiology 2012;23:699–705. PubMed Google Scholar
- Turowski CB, James WD. The efficacy and safety of amoxicillin, trimethoprim-sulfamethoxazole, and spironolactone for treatment-resistant acne vulgaris. Adv Dermatol 2007;23:155–63. PubMed Google Scholar
- Fenner JA, Wiss K, Levin NA. Oral cephalexin for acne vulgaris: clinical experience with 93 patients. Pediatr Dermatol 2008;25:179–83. PubMed Google Scholar
- Andersen JT, Petersen M, Jimenez-Solem E, et al. Trimethoprim use in early pregnancy and the risk of miscarriage: a register-based nationwide cohort study. Epidemiol Infect 2013;141:1749–55. Google Scholar
- Park-Wyllie L, Mazzotta P, Pastuszak A, et al. Birth defects after maternal exposure to corticosteroids: prospective cohort study and meta-analysis of epidemiological studies. Teratology 2000;62:385–92. CrossRef PubMed Web of Science Google Scholar
- Rennick GJ. Use of systemic glucocorticosteroids in pregnancy: be alert but not alarmed. Australas J Dermatol 2006;47:34–6. CrossRef PubMed Google Scholar
- Gur C, Diav-Citrin O, Shechtman S, Arnon J, Ornoy A. Pregnancy outcome after first trimester exposure to corticosteroids: a prospective controlled study. Reprod Toxicol 2004;18:93–101. CrossRef PubMed Web of Science Google Scholar
- Dréno B, Blouin E. [Acne, pregnant women and zinc salts: a literature review]. Ann Dermatol Venereol 2008;135:27–33. PubMed Google Scholar
- Brocard A, Dréno B. Innate immunity: a crucial target for zinc in the treatment of inflammatory dermatosis. J Eur Acad Dermatol Venereol 2011;25:1146–52. PubMed Google Scholar
- Brandt S. The clinical effects of zinc as a topical or oral agent on the clinical response and pathophysiologic mechanisms of acne: a systematic review of the literature. J Drugs Dermatol 2013;12:542–5. PubMed Google Scholar
- Taub AF. Procedural treatments for acne vulgaris. Dermatol Surg 2007;33:1005–26. PubMed Google Scholar
- Hongcharu W, Taylor CR, Chang Y, Aghassi D, Suthamjariya K, Anderson RR. Topical ALA-photodynamic therapy for the treatment of acne vulgaris. J Invest Dermatol 2000;115:183–92. CrossRef PubMed Web of Science Google Scholar
- de Leeuw J, van der Beek N, Bjerring P, Neumann HAM. Photodynamic therapy of acne vulgaris using 5-aminolevulinic acid 0.5% liposomal spray and intense pulsed light in combination with topical keratolytic agents. J Eur Acad Dermatol Venereol 2010;24:460–9. PubMed Google Scholar
- Dréno B, Layton A, Zouboulis CC, et al. Adult female acne: a new paradigm. J Eur Acad Dermatol Venereol 2013;27:1063–70. PubMed Google Scholar
- Purdy S, de Berker D. Acne vulgaris. BMJ Clin Evid 2011;2011. pii. 1714. Google Scholar
Autorzy: Anna L., Chen A., Qi C., Reiner B., Sachs D., Helfrich I. (Uniwersytet Johnsa Hopkinsa, Uniwersytet Michigan, USA)
Na podstawie materiałów JABFM